更新时间:2021-12-10 14:49:45点击:
2021年12月8日,由清华大学医学院教授、清华大学全球健康与传染病研究中心与艾滋病综合研究中心主任张林琦领衔研发的新冠单克隆中和抗体安巴韦单抗/罗米司韦单抗联合疗法(此前称BRII-196/BRII-198联合疗法)获得中国药品监督管理局(NMPA)的应急批准上市,用于治疗新型冠状病毒(SARS-CoV-2)检测结果为阳性,同时伴有进展为重型COVID-19危险因素的成人和青少年(≥12岁,体重≥40 kg)患者。
此获批标志着中国拥有了首个全自主研发并经过严格随机、双盲、安慰剂对照研究证明有效的抗新冠病毒特效药。

张林琦教授表示:“安巴韦单抗/罗米司韦单抗联合疗法的获批,为中国带来了首个新冠治疗特效药。这一联合疗法在国际多中心试验中展现了优异的安全性和保护性,是至今为止在全世界范围内唯一开展了变异株感染者治疗效果评估并获得最优数据的抗体药物。该抗体联合疗法为我国抗击新冠疫情提供了世界一流的治疗手段,充分展示了清华大学在抗击传染病领域的深厚积淀与技术储备,以及召之即来、来之能战、战之能胜的担当与能力,为我国乃至全球疫情防控工作做出了重要贡献。我们非常荣幸与深圳市第三人民医院及腾盛博药在基础、临床和转化研究等方面的高质量合作,取得这一具有里程碑意义的优异成绩,下一步将继续研究单抗联合疗法在高危和免疫缺陷等人群中的预防作用。”
此次获批是基于美国国立卫生研究院(NIH)支持的ACTIV-2的3期临床试验,包括847例入组患者的积极中期及最终结果。最终结果显示,与安慰剂相比,安巴韦单抗/罗米司韦单抗联合疗法能够降低高风险新冠门诊患者住院和死亡风险80%(中期结果为78%),具有统计学显著性。截至28天的临床终点,治疗组为零死亡而安慰剂组有9例死亡,并且其临床安全性优于安慰剂组。同时,无论早期即开始接受治疗(症状出现后5天内)还是晚期才开始接受治疗(症状出现后6至10天内)的受试者,住院和死亡率降低均显著降低,这为新冠患者提供了更长的治疗窗口期。
仅不到20个月的时间,清华大学与深圳市第三人民医院及腾盛博药合作,将安巴韦单抗/罗米司韦单抗联合疗法从最初的中和抗体分离与筛选迅速推进到完成国际3期临床试验,并最终获得中国的上市批准。这一成就是中国与全球一流的科学家和临床研究人员共同努力的成果,包括支持ACTIV-2国际临床研究的美国国立卫生研究院(NIH)下属的美国国家过敏和传染病研究所(NIAID)、以及领导ACTIV-2临床研究的艾滋病临床试验组(ACTG)。
深圳国家感染性疾病临床医学研究中心主任、深圳市第三人民医院党委书记刘磊表示:“从疫情一开始,我们就定下了科技抗疫的目标。我们的研究团队成功从新冠康复期患者的血清中提取了一对高活性的中和抗体,为后续开发这一抗新冠病毒药物打下了坚实的基础。我们很高兴能与清华大学张林琦教授团队及腾盛博药公司合作,为中国首个抗新冠病毒药物贡献出智慧和经验。我们希望在广大科研工作者和医务工作者的共同努力下,我们可以早日战胜新冠疫情。”
腾盛博药总裁兼大中华区总经理罗永庆表示:“我们为实现这一重要里程碑感到兴奋,并正努力推进中国新冠患者对这一联合疗法的可及性。这一成就证明了我们一直坚定不移地致力于加快传染病领域的全球创新,以高效、科学、严谨和优秀的成果来填补未被满足的医疗需求。作为一家在中美两地运营的跨国生物技术公司,我为腾盛博药能取得这样的成绩感到自豪。同时我们也不遗余力地助力中国在复杂多变的新冠疫情中科学应对,满足我国新冠患者的临床需求。”(来源:清华大学)
专题:

城市人口排名:第七次全国人口普查地级市州人口城市排名

2024年硕士及以上中外合作办学机构与项目名单
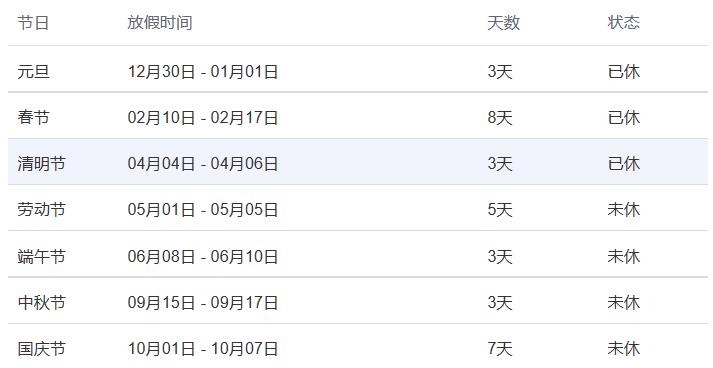
2024年放假时间表及调休时间

什么是市场主体?
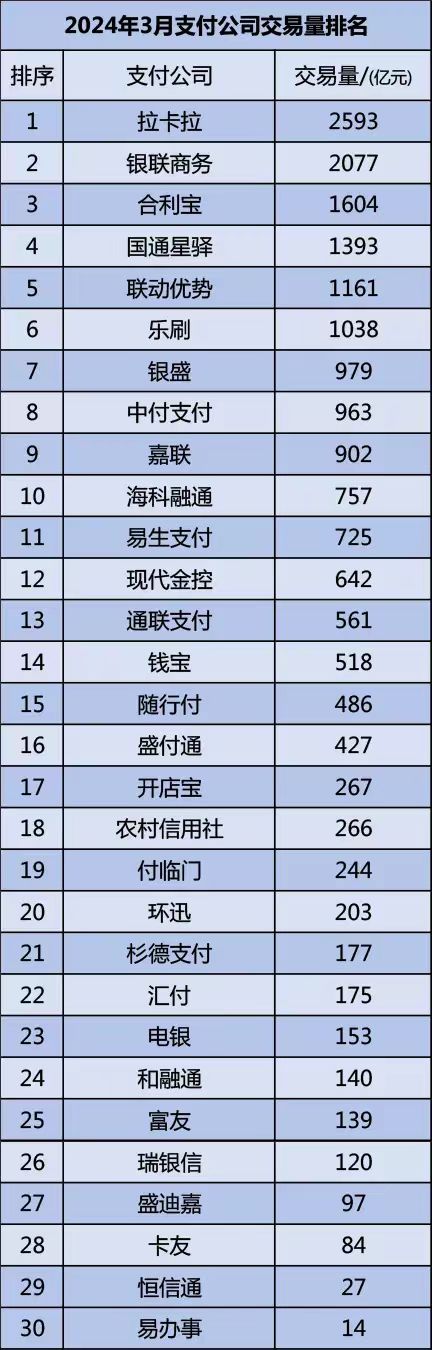
支付公司交易量排名

研究生教育学科专业目录(2022年)

管理类专业硕士包含哪七个专业学位?
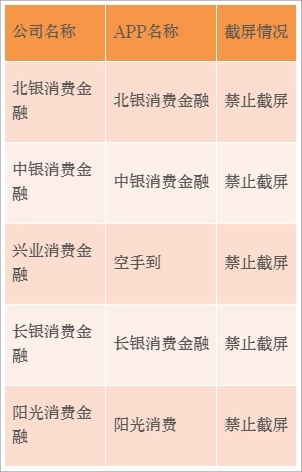
31家消费金融公司利率、APP名称、结清证明通道

如何区分肉桂、水仙、大红袍?

VIP岩茶的品质:滋味、香气

茶事:白毫银针、白牡丹、贡眉、寿眉怎么识别?

2023年福建省各地国民经济和社会发展统计公报汇编
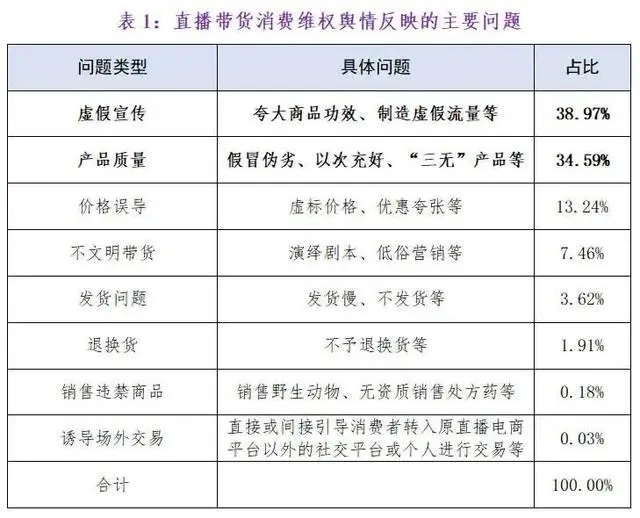
直播带货消费维权舆情反映的主要问题

你的品牌现在处于什么阶段?

微信发布“朋友圈违规避坑指南”——套现、售卖POS机、贷款等服务

新闻发布甄选套餐
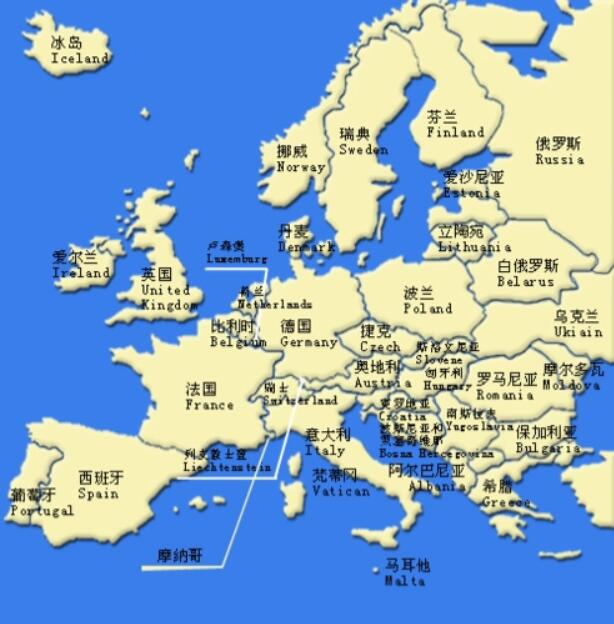
欧洲45个国家分别是哪些?

最新最全已获人民银行许可的支付机构名单
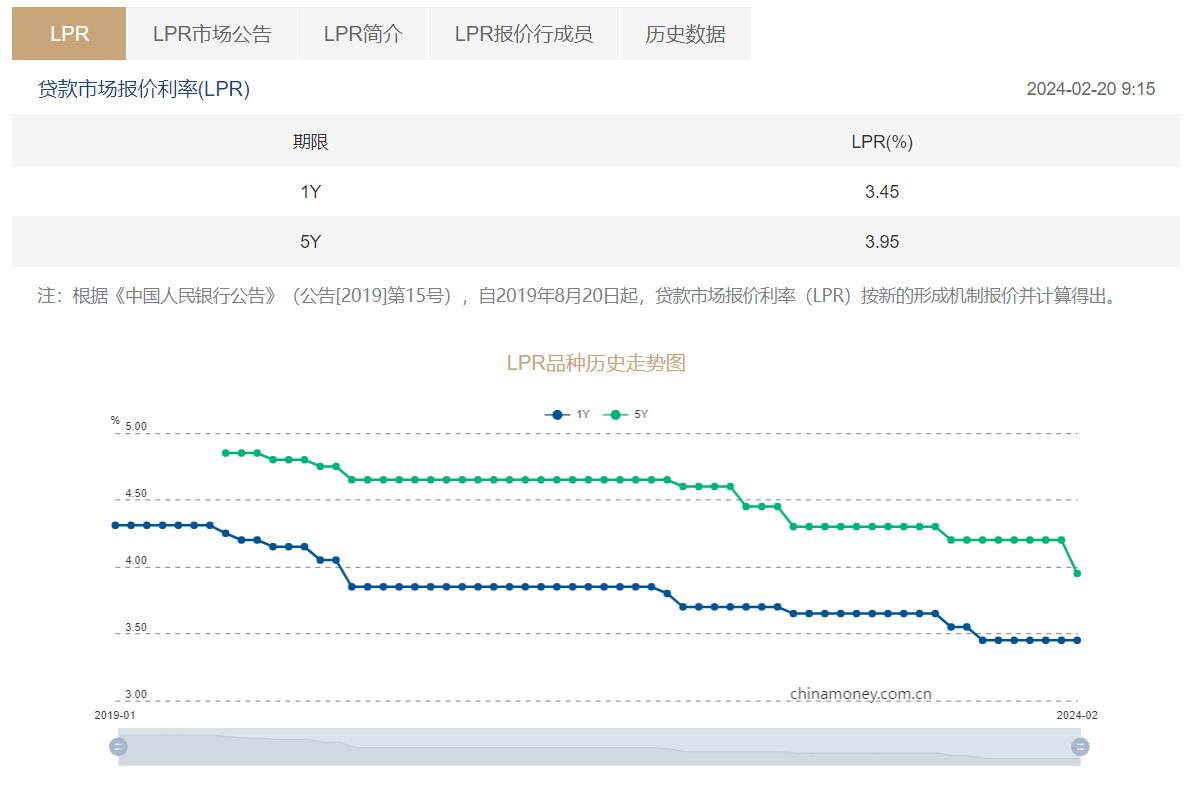
2024年2月1年期LPR为3.45%5年期以上LPR为3.95%

中国主要留学热门国家